Контролируемые атмосферы и установки для их получения
Контролируемые атмосферы и установки для их получения
Окисление металла
При нагреве металлов в печах происходит окисление. Интенсивность окисления будет тем больше, чем выше температура нагрева. Процесс окисления состоит в химическом взаимодействии металла с окислительными газами, находящимися в печной атмосфере.
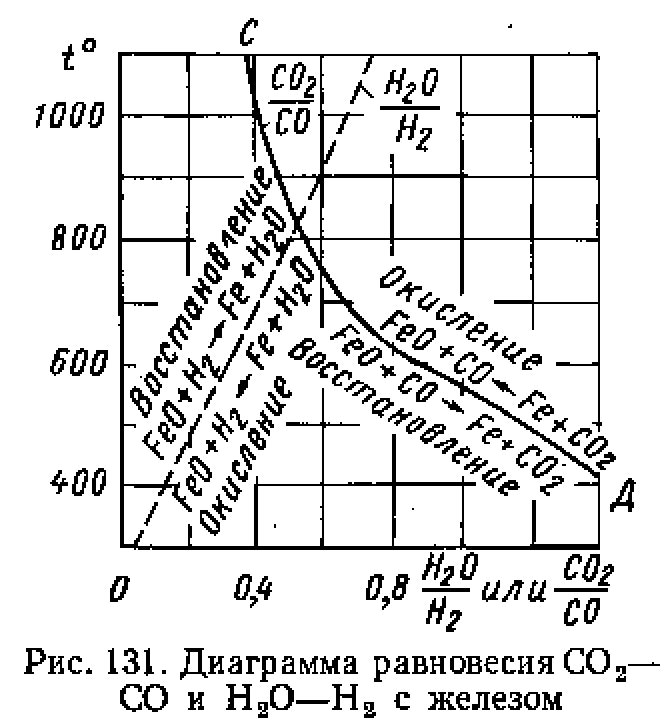
Ход реакций окисления железа водяным ларом и углекислым газом можно проследить по диаграмме, показанной на рис. 131, Если при температуре 1000° С отношение количества водяных паров к водороду будет 6 : 10, то смещение равновесия реакции FeO + НаО пойдет вправо, т. е. с восстановлением железа. Но уже при температуре ниже 900° С железо будет окисляться. Из этой же диаграммы аналогично можно определить, как влияют СО2 и СО на железо и его окисел. При температуре 1000° С и СО®/СО = 6/10 в реакции Fe + СОFeO + СО железо будет окисляться, а при температуре ниже 750° С — восстанавливаться.
Если же в печи присутствуют все четыре газа, то происходит реакция: СО -F Н2Од COS + Н, и соотношение компонентов.
Количество масла, необходимое для охлаждения металла, определяется по формуле.
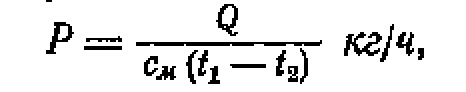

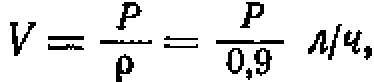

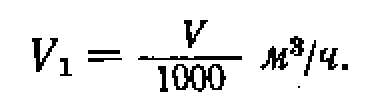
Зная плотность масла, получим объем его смеси, а также окислительная способность газовой смеси изменятся.

Продуктом окисления стали является окалина, состоящая из окислов: FeO, Fe3O4 и FeaO3.
Окислы Fe3O4 и Fe2O3 устойчивы в большом диапазоне температур (от 20 до 1538—1565° С), а окисел FeO устойчив только при температуре выше 570° С до точки его плавления (1377° С). Окисление металла следует рассматривать как процесс двусторонней диффузии окисляющих газов с поверхности внутрь металла через слой окалины [2]. Металл в виде ионов тоже диффундирует сленный слой состоит из Fe2O3 и Fe3O4, но при температурах выше 570° С структура окалины состоит из Fe3O3, Fe3O4 и FeO, причем толщина их примерно соответствует отношению 1:10: 100. Кроме окислительных газов, атмосфера печей содержит восстановительные газы На, СО, СН4 и нейтральный газ N2. Технический азот вследствие постоянного в нем присутствия влаги и до 4% кислорода вызывает окисление стали. При нагреве металла в нейтральной или восстановительной атмосфере окисления не происходит.
Обезуглероживание металла
В процессе нагрева наряду с окислением металла может происходить обезуглероживание поверх- . ностного слоя металла, т. е. уменьшение содержания углерода в поверхностном слое.
Обезуглероживание вызывает изменение механических свойств деталей или заготовок. Кроме того, деталь с обезуглероженной поверхностью склонна к закалочным трещинам, короблению, обладает малой сопротивляемостью статическим нагрузкам и низким пределом усталости. При изготовлении, рессор, например, особенно внимательно следят за обезуглероживанием поверхности рессорных листов, так как с обезуглероженным слоем листы имеют низкий предел усталости и рессоры намного быстрее выходят из строя. При определении обезуглероженного слоя нужно учитывать не только его глубину, но и содержание углерода в нем.
Когда ионы металла достигают внешней поверхности, они реагируют с газом и вследствие избытка кислорода образуют окисел Fe3O3. Кислородные же атомы, проникая внутрь и соединяясь снеокисленным металлом,образуют окисел FeO вследствие избытка металла. Следовательно, можно считать, что снаружи имеется слой Fe3O3, затем Fe3O4, FeO и чистое железо, т. е. окислы располагаются по убывающим степеням окисления.
Обезуглероживанию способствуют: Н2О, СОа, Оа и На. Сущность процесса обезуглероживания заключается во встречной диффузии обезуглероживающего газа и углерода или карбида железа и реакции между ними. Процесс обезуглероживания может происходить по следующим реакциям:
Наиболее обезуглероживающей средой является Н2О, СО2 и На. Но, кроме этого, на процесс обезуглероживания влияет температура нагрева и содержание углерода в стали. Из элементов, способствующих обезуглероживанию, нужно назвать алюминий, кобальт и вольфрам. Хром и марганец задерживают обезуглероживание, а кремний, никель и ванадий не оказывают существенного влияния на обезуглероживание.
Окисление и обезуглероживание происходит в поверхностном слое металла. Обычно обезуглероживание предшествует окислению. Поэтому, если образовалась окалина, то металл защищается от обезуглероживания. Обезуглероживание не является опасным явлением, если детали после термической обработки подвергаются механической обработке со снятием стружки или шлифованию, и обезуглероженный слой полностью снимается. Таким образом, печные газы в рабочем объеме влияют на изменение химического состава и свойств поверхностных слоев стали. Для того чтобы предохранить металл от отрицательного влияния печных газов, в рабочее пространство печи искусственно вводят защитную газовую среду такого состава, который не окисляет и не обезуглероживает металл. Можно также искусственно создать такую атмосферу, которая будет науглероживать металл, как это делается при газовой цементации. Эти газовые среды называются контролируемыми, так как их взаимодействие с металлом при нагреве регулируется в требуемом направлении.
Существует несколько групп контролируемых атмосфер [401: аммиачная, древесноугольная, экзотермическая, эндотермическая, экзо- эндо-, водородная, аргоновая и гелиевая и паровая.
Аммиачная группа
Материалом для получения атмосфер аммиачной группы является безводный жидкий аммиак. Газ (усл. обозн. ДА), получаемый при диссоциации аммиака (2МН3—> ЗНа + + N2), содержит до 75% водорода и является взрывоопасным.
Газ (усл. обозн. ПСА-08), получаемый из продуктов сжигания аммиака с коэффициентом избытка воздуха а = 0,7-5-0,9, Содержит 1 —15%, остальное азот. Этот газ не является взрывоопасным и применяется при отжиге малоуглеродистой стали, а также при нагреве для пайки. Атмосфера аммиачной группы может быть окислительной при наличии водяных паров, и поэтому газ перед пуском в печь сушат путем понижения температуры газовой смеси. При этом происходит понижение равновесного содержания водяного пара, и влажность смеси уменьшается.

Температура,начала конденсации водяных паров из газовой смеси называется точкой росы. Чем ниже эта температура, тем меньше влаги содержится в газовой смеси. Допускаемая влажность газа при отжиге в 0,01% соответствует точке росы — 40° С.
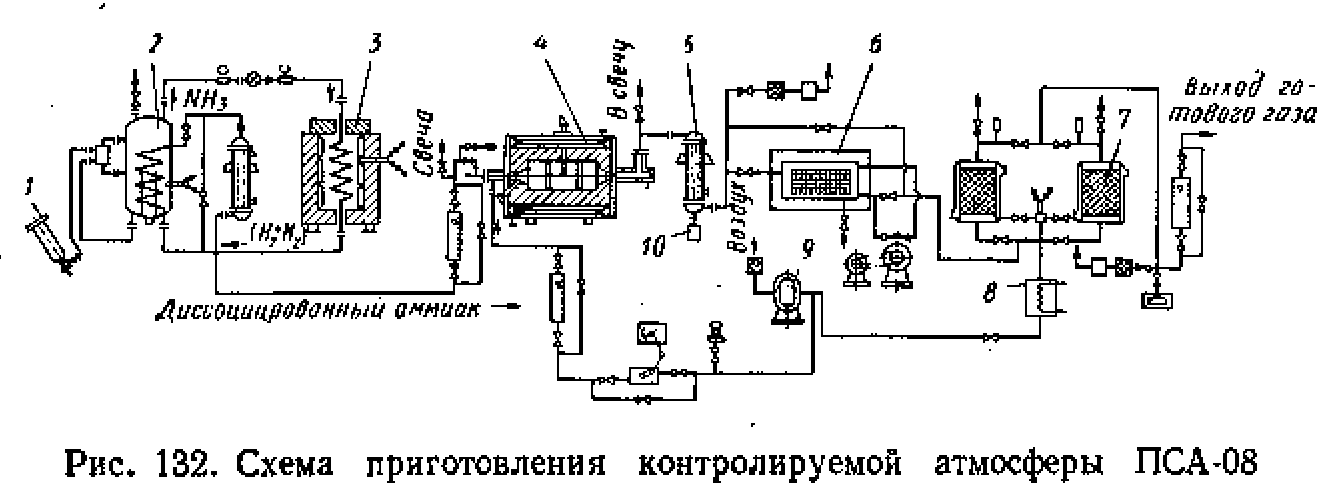
Газ ПСА-08 обезуглероживает средне- и высокоуглеродистые стали. Обезуглероживающее действие этой системы газов вызывается избытком водорода и зависит от направления реакции. Процесс получения контролируемой атмосферы газа происходит по схеме, показанной на рис. 132. Жидкий аммиак из баллонов 1 направляется в испаритель 2, где переходит в газообразное состояние. Отсюда газообразный аммиак поступает в диссоциатор 3 и распадается на водород и азот. Процесс протекает при температуре 600—850° С в присутствии катализатора— железных стружек. После диссоциации газ охлаждается в змеевике испарителя, промывается в скруббере и вводится в камеру 4 частичного сжигания.
Процесс частичного сжигания ведется также в присутствии катализатора—шамотного кирпича с порошком никеля при температуре 900° С. При сжигании соблюдается точное дозирование воздуха и газа. Затем следует охлаждение и сушка газа в скруббере 5, рефрижераторе 6 и адсорбере 7 с силикагелем, после чего газ направляется в печь. Влажность при охлаждении в скрубберах до температуры точки росы (+20° С) составляет 2,3%. При последующем охлаждении в рефрижераторе до температуры +2° С содержание влаги уменьшается до 0,7%. Сушка газа в этом случае происходит вследствие охлаждения газа и конденсации влаги. Окончательная сушка газа ведется в адсорбере с силикагелем. Адсорбер 7 состоит из двух попеременно работающих колонок, заполненных силикагелем (гидратом кремневой кислоты). Процесс поглощения влаги силикагелем идет с выделением тепла, и поэтому работающая колонка охлаждается снаружи водой. В другой колонке в это время происходит восстановление силикагеля путем продувки нагретым до температуры 250—300° С воздухом в течение 2,5 ч. Воздух из воздуходувки 9 подается в камеру частичного сжигания 4 и в нагреватель адсорбера 8. При необходимости газ можно выпускать в атмосферу через водяные затворы 10.
Характеристика, методов осушки газов приведена в табл. 11,
Таблица 11
Характеристика различных методов осушки газа
На рис. 133 показана конструкция установки для изготовления атмосферы из аммиака ДА-ЗОС (ОКБ-674), разработанная во ВНИИЭТО. Вся установка состоит из блоков: испарителя аммиака с диссоциатором, сжигания, охлаждения газа и осушки. В блок испаритель-диссоциатор входят испаритель аммиака, диссоциатор и трубчатый холодильник. Испаритель представляет собой металлический сосуд высокого давления со сферическими днищами и предохранительным клапаном. Испаритель имеет змеевиковый и электрический подогреватели жидкого аммиака. Диссоциатор изготовляют в виде шахтной электропечи, футерованной огнеупорным кирпичом с жароупорной ретортой, заполненной катализатором. Температура контролируется и регулируется автоматически.
Блок Сжигания состоит из камеры сжигания, системы контроля и автоматического регулирования состава газа. В камере находится катализатор горения. Водяная рубашка служит, для отвода избытка тепла от камеры.
Блок охлаждения газа состоит из трубчатого холодильника с гидравлическим затвором, камеры охлаждения с ребристыми охладителями и холодильных установок. Блок сушки состоит из двух силикагелевых осушителей и электрокалорифера для подогрева воздуха. Наружные стенки осушителя охлаждаются водой.

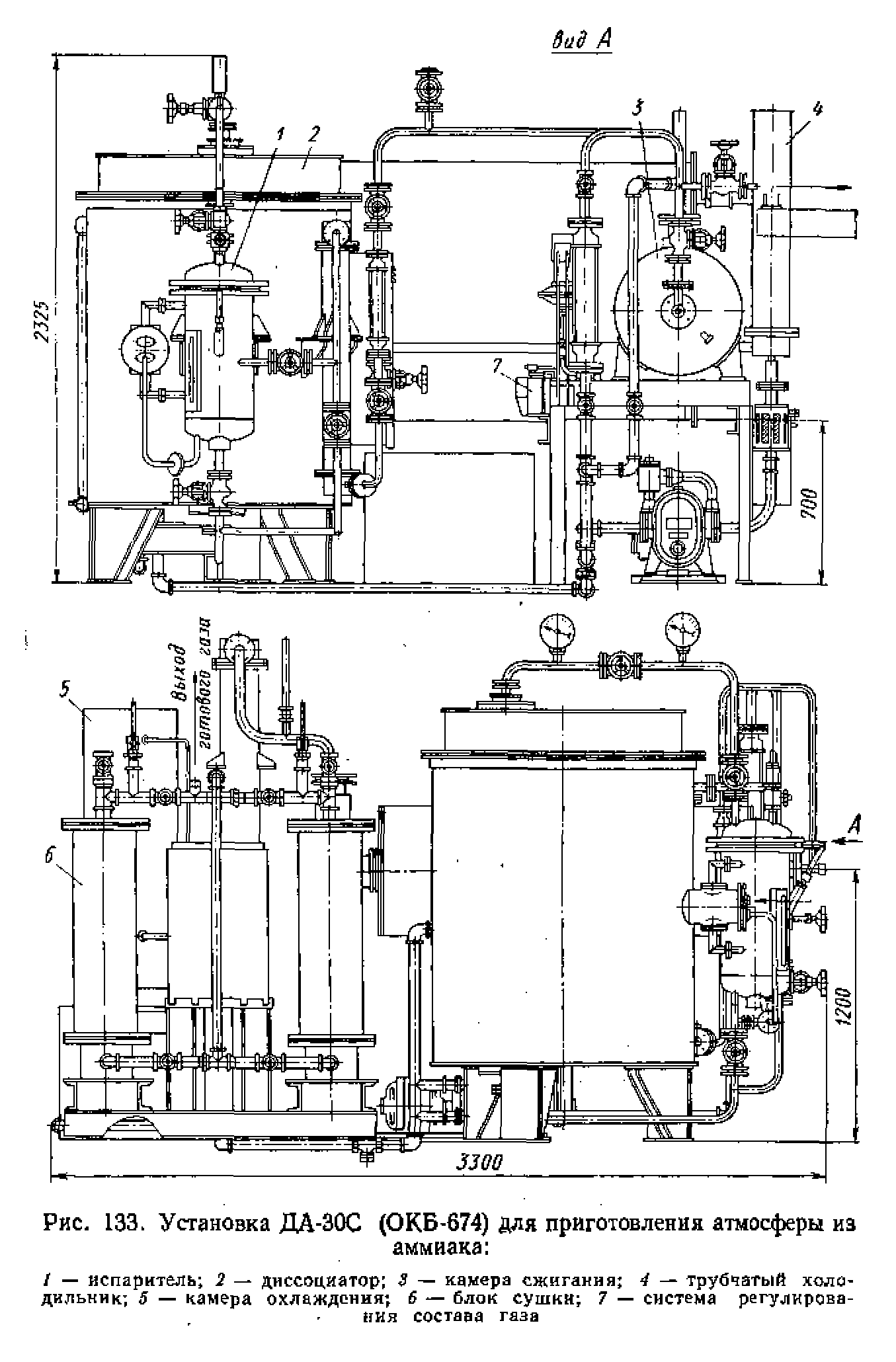
В электрокалорифере находится теплоизоляция и съемный электронагреватель. Ниже приведена техническая характеристика установки ДА-ЗОС
Из отдельных блоков можно составлять установки; например, могут быть смонтированы следующие установки: с диссоциацией аммиака без последующего сжигания, с диссоциацией аммиака с частичным сжиганием, с сушкой или без нее, для очистки технического азота, для частичного сжигания водорода с сушкой или без нее. Кроме того, эти блоки могут быть использованы и для монтажа установок других типов атмосфер.
Существует адсорбент — «молекулярные сита». Такое название адсорбент имеет потому, что размер его пор приближается к размеру молекул. Если размер молекул поглощаемого вещества превышает размер пор адсорбента, то они не проходят и не поглощаются, если же меньше, то они проникают в адсорбент и поглощаются им.
Этот адсорбент представляет собой кристаллическое вещество, сходное с искусственно приготовленными алюмосиликатами — цеолитами. Сушка газа с помощью «молекулярных сит» может быть доведена до точки росы—70-=—80° С. Когда молекулярные сита насыщаются поглощенными веществами, их очищают путем регенерации при температуре 300—350° С.
Молекулярные сита могут быть использованы для избирательного разделения веществ; например, можно отделить НаО от Н2, СОа от Na или остаточный аммиак от смеси Na и Н2, полученных в результате диссоциации NH3.
При использовании молекулярных сит для сушки и разделения веществ конструкции существующих установок с силикагелем или этаноламинами должны быть изменены, так как десорбция поглощенных молекулярными ситами веществ происходит при более высоких температурах, а также изменяются и другие условия — нагрузка, давление, влажность и т. д.
Для приготовления контролируемой атмосферы аммиачной группы можно использовать другую схему. Обезвоженный аммиак испаряется и смешивается с воздухом (1 часть аммиака и 3,6 части воздуха). Смесь пропускается над катализатором, и происходит следующая реакция: 4NH3 + ЗО2 —> 2N2+ + 6НаО + Q (тепло). После этого газ охлаждается и осушивается до точки росы —40° С и ниже. Атмосфера состоит из 99,5—60% Ыа и 0,5—40% Н2. Эта атмосфера находит применение для нагрева высокоуглеродистой лезвийной стали, нержавеющей стали и цветных металлов.

Для получения аналогичных контролируемых атмосфер может быть использован также азот, находящийся в баллонах. Такой азот обычно содержит 3—5% кислорода. Азот смешивается с диссоциированным и охлажденным аммиаком, после чего смесь пропускается над катализатором, способствующим реакции кислорода с водородом при комнатной температуре или продувается через медную стружку и затем осушивается до требуемой точки росы. Можно также пропускать газ через реторту с раскаленным древесным углем. В этом случае в составе атмосферы будет приблизительно 5% СО и остальное Na.
Аммиачная группа атмосфер имеет следующие преимущества: с жидким аммиаком легче обращаться, чем с баллонами газа, эта группа атмосфер почти не имеет посторонних примесей; нетрудно получить диссоциацию аммиака, и газ не требует дальнейшей очистки.
К недостаткам аммиачной группы можно отнести следующее: большие затраты по сравнению с затратами, произведенными для получения других атмосфер; эти атмосферы взрывоопасны в более широком интервале температур, чем другие атмосферы, за исключением атмосфер с невысоким содержанием водорода (до 15%); при содержании в атмосфере незначительного количества недиссо-циированного аммиака происходит нежелательное азотирование стали.
Древесноугольная группа
Древесноугольная группа атмосфер представляет собой генераторные газы, получаемые при пропускании воздуха от вентилятора через нагретый уголь в генераторе. В нижней части камеры генератора уголь сгорает и образует газообразную смесь, состоящую из азота, двуокиси углерода и водяных паров. Эта реакция вызывает сильный нагрев угля в верхней части камеры. Раскаленный уголь вступает в реакцию с двуокисью углерода и превращает его в окись углерода, а водяные пары — в водород. Горячие сухие газы выходят из генератора и направляются через фильтр для очистки. Древесноугольная атмосфера образуется по реакции: 2С + Оа + 3,8Na —* 2СО + 3,8N2.
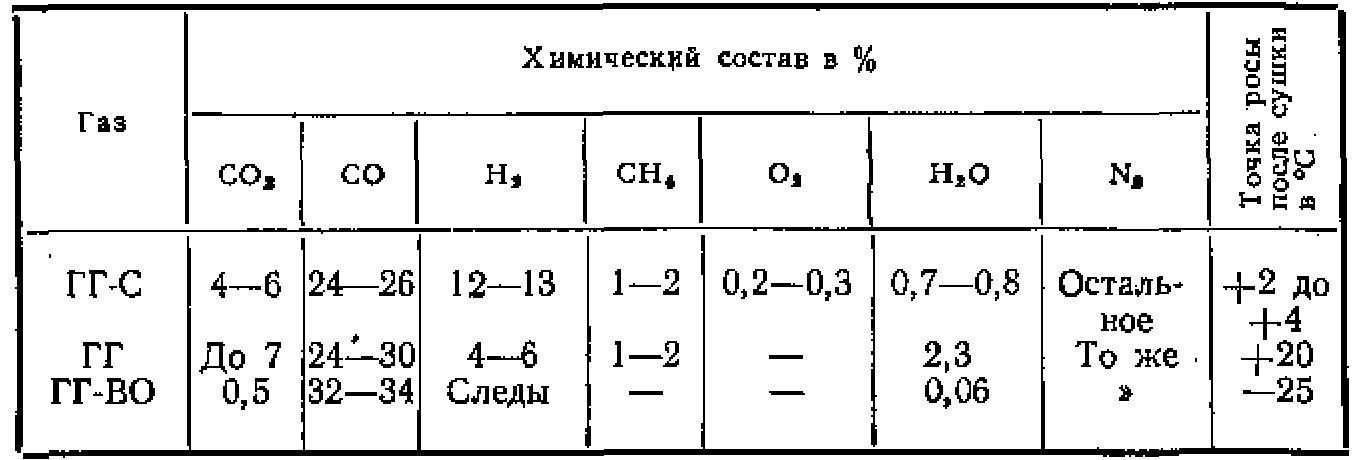
Теоретически по этой реакции в газе должно быть 34% СО и 66% N2. В действительности в результате наличия влаги, летучести древесного угля и неполного превращения двуокиси углерода образуется газовая смесь, содержащая, кроме СО иКг — СОг, Н2, СН4. НаО и даже О2 (табл. 12).
ГГ-С (генераторный газ сухой) — наиболее простой генераторный газ, в который из топлива попадает сера в виде сероводорода, Очистка газа от сероводорода производится в установках с болотной рудой или в скрубберах с водным раствором моноэтано-ламина. Этот газ можно применять для отпуска сталей в широком интервале температур отпуска, для нормализации малоуглеродистой стали и при получении ковкого ферритцогб чугуна.
Примерный состав атмосфер древесноугольной группы в процентах
ГГ (генераторный газ) можно использовать для отжига чугунных отливок на ковкий чугун.
ГГ-ВО (генераторный газ, полученный в генераторе с внешним обогревом) можно применять для нормализации и нагрева при закалке углеродистой и легированной сталей без окисления и обезуглероживания и для отжига цветных металлов,
Безокислительный нагрев обеспечивается при минимальном содержании СОа (до 0,5%); тогда смещение равновесия реакции FeO + СО 7^ Fe + СОа пойдет слева направо. Для предупреждения обезуглероживания необходимо очищать газ от СОа и затем его сушить. Такой очищенный газ обозначается ГГ-0 и применяется для нормализации и закалки среднеуглеродистой и легированной стали. Очистка газа от СОа производится путем пропускания его через абсорбер 1 (50%-ный водный раствор моноэта-ноламина), поглощающий СОа, или через раскаленный уголь.
Раствор моноэтаноламина может быть в дальнейшем восстановлен. Восстановление осуществляется путем нагрева раствора до температуры 98—102° С. При этом происходит обратное выделение (десорбция) СОа, после чего раствор охлаждается и может быть опять использован для поглощения СО2. Таким образом создается замкнутый круг поглощения и выделения углекислоты.
Влажность газа также отрицательно влияет на его свойства. Чем меньше содержания в газе влаги, тем выше может быть концентрация углерода в стали, для которой этот газ применяется. Освобождение газа от влаги (водяных паров) производится промывкой его и пропусканием через холодильник и специальный поглотитель адсорбер. В результате охлаждения конденсируются водяные пары и, таким образом, происходит осушение газа от влаги. Более глубокое осушение происходит при поступлении газа в одну из двух колонок адсорбера с силикагелем, который поглощает влагу. В другой колонке в это время восстанавливается силикагель. Восстановление силикагеля производится путем на-
Таким образом, в процессе реакций литий регенерируется, и его расход составляет 1 г на 1 л газа. Практически это осуществляется путем пропускания газа, прошедшего промывку и предварительное осушение, перед впуском в печь через литиевый испаритель. Реакции происходят при прохождении газа через испаритель, а затем продолжаются в печи.
Содержание СО2 в газе после очистки составляет до 0,1%, влажность газа 0,03—0,04%.
Основными недостатками древесноугольных атмосфер являются: большие затраты, отсутствие подходящих средств для автоматизации контроля, простои при повторных загрузках древесного угля и удаления шлака, коррозия печных деталей генераторов в высокотемпературной зоне сгорания угля. Для получения генераторного газа указанных типов применяют специальные генераторы.
В настоящее время древесноугольные газы в термических цехах машиностроительных заводов почти не применяются. В основном используют природный газ.
Экзотермическая группа
Контролируемые атмосферы, полученные путем переработки природного или сжиженных углеводородных газов, составляют экзотермическую и эндотермическую группы [37]. Для получения эндотермической атмосферы коэффициент избытка воздуха при сжигании исходного газа принимается а = 0,25н-0,40. Для экзотермического газа коэффициент избытка воздуха при сжигании азк = 0,5-ь1,0. Атмосферы с коэффициентом избытка воздуха выше 0,85 являются невзрывоопасными. Состав экзотермических и эндотермических атмосфер в зависимости от коэффициента избытка воздуха при сжигании исходного раза представлен на диаграмме (рис. 134).

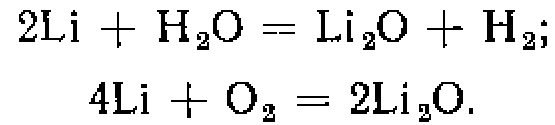
Пары лития способствуют удалению из газа водяных паров. Металлический литий испаряется при относительно низких температурах (около 370° С) и обладает способностью разлагать водяные пары на их составляющие — водород и кислород с поглощением при этом кислорода. Реакция идет следующим образом:
Затем окись лития реагирует с окисью углерода и получается восстановленный литий и углекислый литий, который диссоциирует с образованием СО2 и Li2O:
Экзотермические атмосферы получаются в результате протекания реакций, идущих с выделением тепла, и, следовательно, внешний нагрев реторты генератора не требуется. Получаемые при этом газы можно использовать без очистки от СО2 и Н2О или без очистки от СО2, но с осушиванием газа до точки росы от 4 до —40° С или с очисткой полученных газов от СО2 пропусканием через раствор этаноламинов и осушением силикагелем и, наконец, с очисткой от СО2 и Н2О продуванием через раскаленный уголь.
Экзотермическая группа атмосфер содержит: азота 67-—87%, окиси углерода 1,5—20%, двуокиси углерода 5—11% и водорода 1—1070. В применяемых экзотермических атмосферах часто встречаются следы метана.
Экзотермическая атмосфера может быть богатой или бедной. Богатая атмосфера считается тогда, когда газовоздушная смесь богаче исходным газом, вследствие чего атмосфера характеризуется высоким восстановительным действием. Такая атмосфера имеет более высокое содержание окиси углерода и водорода. Бедная атмосфера содержит небольшой процент этих газов и соответственно более высокое содержание двуокиси углерода и азота. Двуокись углерода в той и другой атмосфере можно удалить путем пропускания газов через раствор моно-этаноламина или через раскаленный уголь. Экзотермические атмосферы наиболее экономичны из всех приготовляемых атмосфер. Они могут применяться для светлого отжига черных и цветных металлов, для светлой нормализации и светлого отпуска, если обезуглероживание для данной стали не существенно.
Экзотермические атмосферы имеют углеродный потенциал менее чем 0,1 %. Поэтому они не пригодны для светлого отжига или закалки углеродистых и легированных сталей, для которых обезуглероживание является важным фактором. Экзотермические атмосферы не могут быть пригодны для светлого отжига нержавеющих сталей, так как их составляющие СО2 и водяные пары окисляют; СО также окисляет хром. Для получения экзотермических атмосфер приготовляют газовоздушную смесь с коэффициентом избытка воздуха а = 0,5-f1,0. Однако получаемые продукты сгорания содержат высокий процент СО2 (табл. 13).
Газы ПС-06 и ПС-09 для операций термической обработки не применяются. Если газ ПС-06 подвергнуть охлаждению в рефрижераторе до точки росы 4° С, получается сухой газ (ПСС-06).